5 月 27 日,卫材药业宣布,「莱博雷生片」(商品名:达卫可)在中国获批上市,用于治疗成人失眠。
值得一提的是,莱博雷生是国内首款获批上市的双重食欲素受体拮抗剂,其获批意味着国内失眠患者迎来了全新机制的新疗法。

图源:企业官微
莱博雷生由卫材药业研发,通过竞争性结合两种食欲素受体亚型(OX1R 和 OX2R),抑制食欲素神经传递,调节睡眠-觉醒节律。莱博雷生对 OX2R 具有更强的抑制作用,可抑制快速眼动睡眠(REM)和非 REM 睡眠驱动,实现更快的睡眠开始和更好的睡眠维持。
据 Insight 数据库显示,该药最早于 2019 年 12 月在美国获批上市,商品名为 Dayvigo。目前,已经在超过 15 个国家和地区获批上市,包括日本、加拿大、澳大利亚等。
在中国,2021 年度莱博雷生率先在中国香港和中国台湾上市,中国内地的首项上市申请则在 2024 年 1 月正式获 CDE 受理。但在本次获批之前,得益于「港澳药械通」政策,莱博雷生片得以新增进第四批粤港澳大湾区内地临床急需进口港澳药品医疗器械目录,从而可在指定医疗机构开具处方。
在本次获批之后,更大范围的中国患者将受惠于此款新疗法。
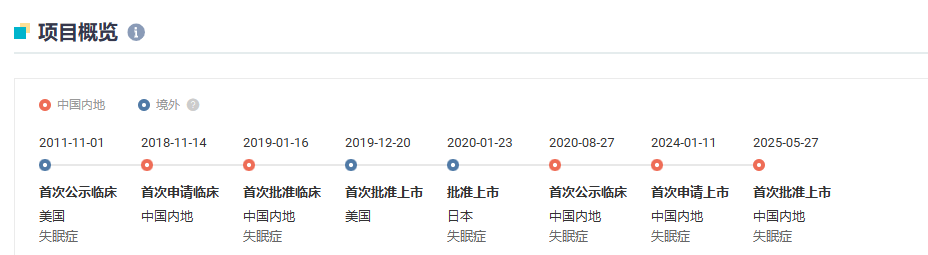
项目开发关键节点
图源:丁香园 Insight 数据库
目前,莱博雷生在中国内地和中国台湾开展的 III 期临床试验(NCT04549168/CTR20190248)尚未公布结果,不过两项 III 期全球临床 SUNRISE 1(NCT02783729)和 SUNRISE 2(NCT02952820)都已有结果发布。
SUNRISE 2 是一项为期 12 个月的随机、双盲、平行全球多中心 III 期研究,包括 6 个月的安慰剂对照期和随后 6 个月的积极治疗期。试验共纳入 949 名成人失眠患者,随机接受安慰剂或莱博雷生(5mg 或 10mg)。
结果显示,与安慰剂相比,莱博雷生组患者报告的入睡潜伏期和入睡后主观觉醒时间均从基线减少,而主观睡眠效率从基线增加。具体而言,5mg 莱博雷生使患者主观睡眠开始潜伏期(sSOL)减少了 26.8 分钟,10mg 组患者减少了 32.1 分钟,而安慰剂组仅减少 17.5 分钟。在次要终点主观总睡眠时间(sTST)上,5mg、10mg 莱博雷生分别为 81.2 分钟、93.2 分钟,而安慰剂组仅为 74.8 分钟。
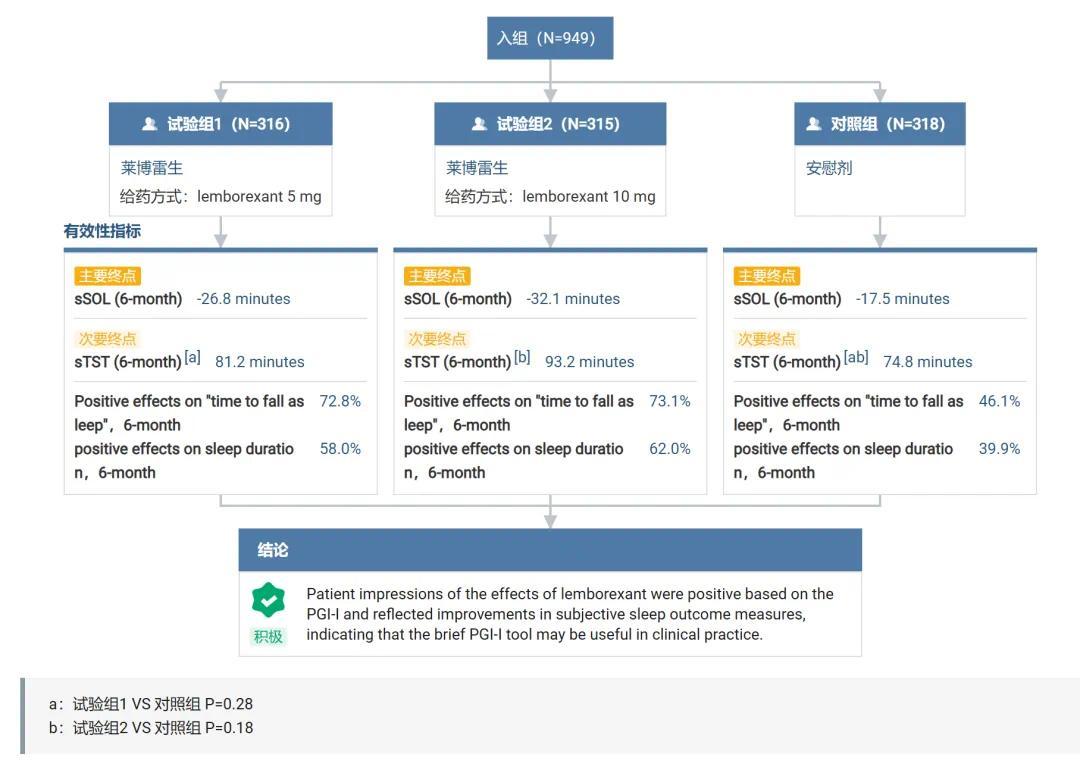
SUNRISE 2 研究结果
图源:丁香园 Insight 数据库
国内失眠人群庞大,中国睡眠数据报告统计,2025 年,中国有超过 5 亿人存在睡眠困扰。
然而,目前的治疗药物主要以苯二氮卓类镇静催眠药(地西泮、艾司唑仑等)、非苯二氮卓类镇静催眠药(唑吡坦、扎来普隆等)、褪黑素受体激动剂(如雷美替胺、阿戈美拉汀)和具有催眠效应的抗抑郁药物(如多塞平、氟伏沙明)。然而这些药物多为老药,且存在耐药性、药物依赖性、反弹性失眠等问题。
食欲素受体拮抗剂作为一种全新机制,有望突破这些困难,为患者带来新治疗方案。Insight 数据库显示,在莱博雷生之后,爱可隆制药/先声药业的「达利雷生」、扬子江药业的「法赞雷生」也分别在去年 7 月、今年 1 月陆续提交了上市申请。
编辑:ccai
编辑:ccai
